Annuncio di una sperimentazione clinica per la malattia di Huntington: un farmaco che riduce l’huntingtina entrerà nella fase I di sperimentazione nel 2015
Per il 2015 è prevista una sperimentazione clinica per un’entusiasmante terapia contro la MH. Il primo passo è assicurarsi che sia sicura.

Una nuova sperimentazione clinica appena annunciata per il 2015 mira a testare una terapia di “riduzione dell’huntingtina”, chiamata oligonucleotide antisenso (ASO), che attacca direttamente l’huntingtina mutante. Siamo estremamente entusiasti: è la prima sperimentazione umana sulla MH in assoluto a combattere la MH alla radice del problema e si è dimostrata molto promettente nei modelli animali. Qual è la novità?
Un potenziale farmaco che prende di mira il gene della MH
La sperimentazione clinica annunciata rappresenta una collaborazione tra Isis Pharmaceuticals, con sede in California, e il gigante farmaceutico svizzero Roche. Il farmaco, chiamato ASO-HTT-Rx, è una terapia che mira a trattare la MH prendendo di mira il gene stesso.
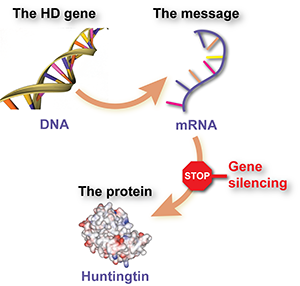
Il nocciolo del problema nella MH risiede in un tratto difettoso di DNA: un tratto extra lungo di elementi costitutivi CAG all’interno del gene huntingtin. Le istruzioni contenute nel gene mutante vengono prima copiate in una copia intermedia di ‘messaggero’, dalla quale viene prodotta la proteina dannosa. Quindi, il gene mutante è la radice del problema, ma è negativo solo perché le cellule usano le informazioni nel gene per produrre una proteina dannosa.
La strategia alla base di ASO-HTT-Rx è quella di “sparare al messaggero”, attaccando la fase intermedia tra gene e proteina causando la distruzione della copia del messaggero.
Questi tipi di farmaci sono chiamati ‘oligonucleotidi antisenso’, o ASO. Sono una molecola sintetica simile al DNA che può entrare nelle cellule, aderire al messaggio di RNA dell’huntingtina mutante e causarne la degradazione. Se funziona come previsto, questa terapia impedirà la produzione della proteina huntingtin, una strategia di “riduzione dell’huntingtina” che, a lungo termine, ha il potenziale per rallentare o arrestare la progressione della malattia.
Ogni ASO ha una struttura di base che può essere modificata per aiutarlo ad aderire al giusto messaggio target, ignorando le migliaia di altri messaggi nella cellula. È un po’ come quando vai al negozio di ferramenta per farti copiare una chiave: il commesso seleziona la chiave vergine corrispondente e poi incide la sequenza corretta di scanalature per adattarsi alla tua serratura, ma a nessuna delle serrature dei tuoi vicini. Nel caso degli ASO, gli scienziati di Isis utilizzano una delle loro molecole ‘backbone’ consolidate e la personalizzano, facendo sì che il farmaco attacchi solo il messaggio dell’Huntingtina.
Tutto questo sembra una tecnologia all’avanguardia, ma la grande notizia è che Isis ha già testato farmaci a base di ASO nel cervello umano, in trattamenti sperimentali per la SLA (Sclerosi Laterale Amiotrofica, o malattia del motoneurone) e la SMA (atrofia muscolare spinale), e non sono stati segnalati problemi di sicurezza.
Somministrazione del farmaco
Un modo importante in cui gli ASO differiscono dai trattamenti farmacologici convenzionali è che non possono essere assunti per via orale come una pillola, ma devono essere somministrati direttamente al sistema nervoso.
Per entrare nel cervello, ASO-HTT-Rx sarà somministrato tramite un ago inserito nello spazio pieno di liquido sotto il midollo spinale inferiore. Se sembra estremo, state certi che questo metodo è usato di routine in molte aree della medicina. Una strategia simile è usata dai medici oncologi per somministrare farmaci chemioterapici a pazienti con tumori cerebrali. Più comunemente ancora, molte donne ricevono una simile somministrazione ‘epidurale’ di farmaci antidolorifici durante il parto.
Un vantaggio importante di farmaci come ASO-HTT-Rx è che i ricercatori ritengono che possa essere somministrato a intermittenza e rimanere efficace. Gli scienziati hanno soprannominato questo approccio al trattamento intermittente nella MH una ‘vacanza dell’huntingtina’; con l’obiettivo di dare al cervello una pausa di guarigione dal danno causato dalla proteina huntingtin mutante.
Una volta iniettato nel liquido spinale, ci vogliono circa 4-6 settimane perché ASO-HTT-Rx abbia il suo effetto, e dagli studi sugli animali pensiamo che il silenziamento durerà poi per circa 4 mesi. Al momento, lo studio è progettato per far ricevere ai pazienti il trattamento farmacologico una volta al mese.
“Farmaci simili a ASO-Htt-Rx hanno ripristinato in modo sicuro comportamenti sani in modelli animali di MH, e spostare il trattamento negli esseri umani è un passo entusiasmante per l’intera comunità MH. Per quanto entusiasmante sia questa scienza, la prima sperimentazione pianificata è strettamente progettata per capire se il farmaco è sicuro.”
La sicurezza prima di tutto
La decisione di andare avanti con una sperimentazione clinica a partire dal 2015 è il risultato di più di dieci anni di lavoro che coinvolge molti ricercatori sia nel mondo accademico che nell’industria. Quando trattati con ASO-Htt-Rx, i topi di laboratorio che modellano la MH mostrano robusti benefici, anche trattandoli con ASO dopo che mostrano i sintomi si verificano miglioramenti nel loro cervello e nel loro comportamento.
I ricercatori di Isis e la prof.ssa Sarah Tabrizi, University College London e responsabile globale dello studio ASO-HTT-Rx, sottolineano che questa prima sperimentazione clinica è progettata esclusivamente per valutarne la sicurezza.
Questo è un punto critico. Per quanto entusiasmante sia questa scienza, la prima sperimentazione pianificata è strettamente progettata per capire se il farmaco è sicuro. Iniettare direttamente qualsiasi farmaco nel sistema nervoso non può essere fatto alla leggera: tutti i potenziali rischi ed effetti collaterali devono essere esaminati in modo esaustivo in un piccolo numero di pazienti volontari.
Anatomia di una sperimentazione clinica
Tutte le sperimentazioni cliniche di fase I mirano prima di tutto a valutare la sicurezza e la tollerabilità di nuovi farmaci. Questo significa che un piccolo gruppo di pazienti (probabilmente circa 36) sarà trattato con diverse quantità di ASO-Htt-Rx, al fine di determinare se il farmaco ha effetti collaterali avversi e per aiutare a trovare la dose ottimale.
Circa il 25% dei pazienti coinvolti riceverà un’iniezione di placebo (una che non contiene alcun farmaco) per servire come gruppo di confronto. I medici monitoreranno i sintomi dei pazienti in risposta al trattamento, ma l’obiettivo principale di questa sperimentazione è capire se il nuovo farmaco è sicuro.
Una volta che un farmaco è stato ritenuto sicuro nella fase I, può progredire alla fase II. È in questo secondo passo che i medici possono reclutare un numero maggiore di pazienti e iniziare a esaminare quanto sia efficace il farmaco nel trattamento dei sintomi della malattia. Avendo stabilito la sicurezza e la dose nella prima sperimentazione, i ricercatori possono ora porre la domanda: ‘questo trattamento migliora (o peggiora!) i sintomi della MH delle persone’?
Se i risultati della sperimentazione di fase II sono positivi, una sperimentazione di fase III coinvolge un numero ancora maggiore di pazienti, esaminando attentamente gli effetti collaterali, l’efficacia e la sicurezza del farmaco. Una sperimentazione di fase III di successo è il tipo di risultato di cui le aziende farmaceutiche hanno bisogno per ottenere l’approvazione di un farmaco da parte delle agenzie di regolamentazione nazionali.
Image credit: Shutterstock
Cosa significa questo per i pazienti con MH?
L’intero processo di immissione di un farmaco sul mercato richiede anni, anche se tutto va perfettamente. Se ASO-Htt-Rx si rivela sicuro nello studio di fase I appena annunciato, questo primo risultato è solo l’inizio di un lungo percorso nella clinica. Ogni sperimentazione lungo quel percorso, fasi I, II e III, coinvolgerà un numero relativamente piccolo di pazienti trattati. Inoltre, all’interno di ciascuna di queste sperimentazioni, alcuni dei volontari riceveranno un trattamento placebo per servire come confronto per i pazienti che ricevono HTT-ASO-Rx.
I pazienti nella sperimentazione di fase I di HTT-ASO-Rx saranno reclutati solo da alcuni centri medici in Europa e Canada. Un piccolo gruppo di centri di ricerca MH designati, che saranno annunciati all’inizio del 2015, cercherà di reclutare i partecipanti alla sperimentazione. Le reclute saranno persone nelle prime fasi della MH, ma i criteri specifici di arruolamento, i luoghi e i tempi non sono ancora informazioni pubbliche. Sappiamo per certo che molta pianificazione dettagliata sta avvenendo dietro le quinte e che tutti stanno lavorando molto duramente per far progredire questa sperimentazione il più rapidamente possibile.
Sicurezza, incertezza, speranza
In sintesi, siamo entusiasti che la prima sperimentazione umana di un farmaco che prende di mira la causa principale della MH inizierà già il prossimo anno. Questo entusiasmo è temperato dalla consapevolezza che questa prima sperimentazione riguarda solo la sicurezza, coinvolge solo un numero molto piccolo di pazienti con MH e che molti dettagli dello studio sono ancora incerti.
Farmaci simili a ASO-Htt-Rx hanno ripristinato in modo sicuro comportamenti sani in modelli animali di MH, e spostare il trattamento negli esseri umani è un passo entusiasmante per l’intera comunità MH. Seguiremo i progressi della sperimentazione con occhio attento, in modo da poter fornire, si spera, dosi intermittenti di cauto ottimismo.
Per saperne di più
- Link al sito web di Isis Pharmaceuticals, sviluppatore della terapia ASO-HTT-Rx
- HDBuzz intervista la prof.ssa Sarah Tabrizi, responsabile globale della sperimentazione terapeutica ASO-HTT-Rx
- Discorso scientifico della prof.ssa Sarah Tabrizi al meeting del 2014 dell’European Huntington’s Disease Network che annuncia il lancio della sperimentazione ASO-HTT-Rx
Fonti e Riferimenti
Per maggiori informazioni sulla nostra politica di divulgazione, consulta le nostre FAQ…


