
Le cellule staminali “indotte” compiono entusiasmanti progressi
Cellule staminali di pazienti affetti da HD: stanno diventando strumenti importanti per i ricercatori e ora correggono la mutazione dell’HD in laboratorio

Le cellule staminali sono fonte di grande entusiasmo per i pazienti affetti da malattie causate dalla morte di cellule nel corpo, come la malattia di Huntington. Ma il diavolo si nasconde nei dettagli e l’utilizzo effettivo di queste potenti cellule per aiutare i pazienti affetti da HD è un problema complesso. Ora, due nuovi studi hanno promosso le cellule staminali come strumento per i ricercatori e dimostrano che è possibile, nelle cellule in una capsula di Petri, correggere la mutazione che causa l’HD.
Aggiornamento sulle cellule staminali
Tutti gli esseri umani sono nati come un singolo ovulo fecondato, che si divide ripetutamente per formare i circa 50 trilioni di cellule presenti nell’uomo adulto. Ogni cellula ha le sue proprietà: le cellule muscolari funzionano in modo molto diverso dalle cellule della pelle e così via. Le proprietà speciali di ogni tipo di cellula determinano quali funzioni quella cellula può svolgere.
Credito immagine: PNAS
Per molti anni, gli scienziati hanno creduto che solo un tipo molto speciale di cellula, chiamata cellula staminale, fosse in grado di dividersi e dare origine ai diversi tipi di cellule del nostro corpo. La fonte più ovvia di queste cellule erano gli embrioni allo stadio iniziale, dove si trovano normalmente. Sebbene queste “cellule staminali embrionali” fossero estremamente potenti, consentendo agli scienziati di far crescere nuove cellule come le cellule cerebrali in laboratorio, il loro uso era eticamente e legalmente difficile perché richiedeva la distruzione di embrioni.
Nel 2006 tutto ciò che sappiamo sulle cellule staminali è cambiato, quando Shinya Yamanaka ha scoperto la capacità di “riprogrammare” qualsiasi cellula adulta in una cellula staminale. Improvvisamente, non c’era più bisogno di distruggere embrioni per creare cellule staminali: potevamo semplicemente prelevare un piccolo campione di pelle e riprogrammare le cellule presenti nella pelle per farle diventare cellule staminali. Gli scienziati sono diventati abbastanza bravi a far crescere neuroni, cellule muscolari e altri tipi critici di cellule danneggiate in varie malattie a partire da cellule staminali, una volta che le hanno a disposizione.
Queste cellule riprogrammate sono chiamate cellule staminali pluripotenti indotte, o cellule iPS.
Il nostro manuale di base sulle cellule staminali ha precedentemente esaminato l’entusiasmo e le difficoltà della ricerca sulle cellule staminali per la malattia di Huntington.
Cellule staminali di pazienti affetti da HD
In un articolo appena pubblicato sulla rivista dal nome un po’ strano “Cell Stem Cell”, un gruppo collaborativo di scienziati ha creato e studiato una serie di queste cellule staminali pluripotenti indotte da pazienti affetti da HD. I ricercatori erano curiosi di sapere se le cellule staminali di pazienti affetti da HD si sarebbero comportate in modo diverso da quelle di persone che non sono portatrici della mutazione.
Il gruppo di scienziati ha esaminato come si comportavano le cellule in laboratorio. Diversi decenni di lavoro hanno suggerito che le cellule di pazienti affetti da HD sono anormali, ma nessuno è mai stato in grado di studiare le cellule staminali a questo livello di dettaglio prima, perché sono state così difficili da ottenere.
Si scopre che le nuove linee di cellule staminali create da pazienti affetti dalla malattia di Huntington si comportano in modo diverso dalle cellule staminali create da persone senza HD. Le principali differenze riguardavano il modo in cui le cellule attivavano e disattivavano i geni e il modo in cui producevano energia.
Questi sintomi cellulari corrispondono in gran parte alle osservazioni che gli scienziati hanno fatto in altri tipi di cellule con la mutazione della malattia di Huntington, suggerendo che queste nuove cellule staminali saranno uno strumento davvero utile per capire come la mutazione altera la funzione delle cellule, portando infine alla loro morte precoce nell’HD.
Qual è il punto di tutto questo? Cosa possono aspettarsi i pazienti affetti dalla malattia di Huntington da queste nuove linee cellulari? Il contributo più importante delle cellule staminali di pazienti affetti da HD è la fornitura di un modello per gli scienziati che studiano la malattia.
Immagina di essere un’azienda farmaceutica che crede che il tuo nuovo farmaco aiuterà le cellule a far fronte alla mutazione della malattia di Huntington e a rimanere sane più a lungo. Ora, grazie a queste nuove cellule staminali, puoi testare il tuo farmaco in cellule cerebrali prodotte da pazienti affetti da HD, piuttosto che in cellule di un topo o di un verme. Si spera che questo fornisca risultati molto più accurati e ci aiuti a testare solo farmaci veramente efficaci nelle persone.
Sostituzione cellulare?
Un sogno per molti ricercatori e persone che convivono con la malattia di Huntington è che un giorno potremmo sostituire le cellule perse con nuove, permettendoci di fermare, o forse anche invertire, i sintomi delle malattie degenerative.
La crescita di nuove cellule per sostituire quelle perse in una malattia è nota come terapia di sostituzione cellulare, ed è uno dei motivi di tutto l’entusiasmo che circonda le cellule staminali. Alcuni ricercatori ritengono che il trapianto di cellule staminali nelle parti danneggiate del cervello di pazienti affetti da HD potrebbe sostituire quelle cellule che muoiono durante il corso della malattia.
Sarà necessario superare importanti sfide scientifiche prima che la terapia di sostituzione cellulare possa funzionare. Innanzitutto, quali cellule dovremmo inserire nel cervello delle persone? Ovviamente, vorremmo sostituire le cellule cerebrali morenti con altre cellule cerebrali, non con cellule della pelle o cellule muscolari. Quindi, dove possiamo trovare altre cellule cerebrali e come possiamo assicurarci che siano una “corrispondenza” genetica per il paziente?
È qui che entrano in gioco queste nuove cellule staminali “indotte”: per la prima volta potremmo teoricamente prelevare un campione di pelle da un paziente affetto da HD, riprogrammare le cellule per farle diventare cellule staminali o neuroni e iniettare quelle cellule staminali nel cervello del paziente stesso. Se funzionasse, questa sarebbe un’opzione fantastica perché le cellule sarebbero una corrispondenza genetica esatta per il paziente.
Recenti esperimenti su un ratto suggeriscono che le cellule staminali iniettate in questo modo possono formare nuove cellule cerebrali che sembrano integrarsi nel cervello e aiutare i ratti a riprendersi da danni cerebrali.
Correzione della mutazione dell’HD
I lettori più attenti potrebbero aver notato un problema qui: la mutazione che causa l’HD si trova in ogni cellula del nostro corpo, comprese le cellule della pelle e le cellule staminali che produciamo da esse. Quindi, anche se affrontiamo con successo le sfide tecniche della somministrazione di cellule staminali nel cervello, ci ritroviamo con nuovi neuroni che hanno la stessa mutazione che causa l’HD in primo luogo!
La soluzione ideale a questo problema sarebbe se potessimo “riparare” le cellule staminali di pazienti affetti da HD rimuovendo la mutazione che causa l’HD, mentre le cellule crescono in una capsula di Petri. Esistono alcune tecniche molto nuove per fare proprio questo: abbiamo precedentemente trattato una tecnologia, chiamata nucleasi a dita di zinco. Ma queste tecnologie sono nuove e probabilmente mancano molti anni all’applicazione nei pazienti affetti da HD.
Un gruppo di scienziati guidato da Lisa Ellerby presso il Buck Institute for Research on Aging ha considerato un altro approccio a questo problema. Apportare modifiche precise ai geni delle cellule staminali che crescono in una capsula di Petri è molto, molto più facile che modificare il DNA di persone viventi. Infatti, il processo viene utilizzato regolarmente per produrre i topi geneticamente modificati utilizzati per studiare la biologia e la medicina nei laboratori di tutto il mondo.
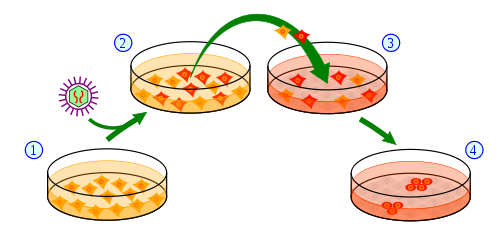
Il gruppo di Ellerby ha fatto un esperimento molto semplice: ha dato alle cellule staminali di un paziente affetto dalla malattia di Huntington un po’ di DNA extra che diceva loro come produrre un gene HD normale, piuttosto che mutante.
L’efficienza di questa procedura è estremamente bassa: di 5 milioni di cellule trattate, solo 2 cellule hanno utilizzato il DNA extra per apportare la correzione appropriata. Ma usando un marcatore luminoso per etichettare quelle cellule che hanno effettivamente apportato la correzione, potevano essere isolate e coltivate.
Questo semplice trucco genetico ha permesso a Ellerby e al suo gruppo di fare una serie sorprendente di confronti. Potevano porre domande come: qual è la differenza tra una cellula con una mutazione HD e la stessa identica cellula con la mutazione corretta? Il suo team, come il consorzio di cellule staminali, ha esaminato i decenni di lavoro sull’HD nelle cellule e ha studiato cosa è successo alle cellule HD che sono state “riparate”. Questa analisi ha rivelato che alcune delle anomalie nelle cellule HD possono essere corrette riparando la mutazione HD.
Problema risolto?
Questo fornisce informazioni importanti agli scienziati che studiano la malattia di Huntington. Ma potrebbe essere altrettanto importante per risolvere il problema del trattamento: come facciamo a far sì che le nuove cellule siano adatte a sostituire le cellule perse nell’HD?
Tornando ora a questo problema, possiamo vedere che ora è possibile, in teoria, riprogrammare le cellule della pelle di un paziente affetto da HD in cellule staminali. Quelle cellule staminali potrebbero quindi essere geneticamente “corrette”, rimuovendo la mutazione che causa l’HD dal loro genoma. L’impianto di quelle cellule geneticamente modificate consentirebbe, in teoria, a nuovi neuroni di crescere nel cervello dei pazienti, privi della mutazione HD.
Qui a HDBuzz, siamo lieti della velocità di questi progressi nelle cellule staminali e delle possibilità di trattamenti per l’HD. Ma riteniamo anche che lo sviluppo di questi notevoli progressi in trattamenti per l’HD sarà ancora un processo molto lungo e difficile, infatti, molto più difficile dello sviluppo di un farmaco tradizionale.
La somministrazione di cellule geneticamente modificate nel cervello di pazienti viventi è molto rischiosa e dovrà essere affrontata con grande cautela. Probabilmente ci vorranno molti anni di studi di laboratorio sempre più sofisticati prima che questo metodo di trattamento venga utilizzato su larga scala nelle persone.
In un arco di tempo molto più breve, tuttavia, questi importanti progressi nelle cellule iPS saranno probabilmente strumenti molto utili per comprendere la malattia di Huntington e semplificare il processo di sviluppo dei farmaci. Nel frattempo, le cellule staminali come trattamenti si stanno muovendo lentamente lungo il percorso delle terapie in fase di sviluppo per l’HD. Mentre altri trattamenti con tempi più brevi superano le sperimentazioni, è fondamentale iniziare lo sviluppo di queste tecnologie a più lungo termine ma estremamente promettenti.
Per saperne di più
- Pubblicazione originale dell’HD iPSC Consortium su Cell Stem Cell (l’articolo completo richiede il pagamento o l’abbonamento)
- Pubblicazione originale di An, Ellerby e colleghi su Cell Stem Cell sulla correzione del difetto genetico nelle cellule staminali HD (l’articolo completo richiede il pagamento o l’abbonamento)
- La nostra recensione del settore delle cellule staminali per i pazienti affetti da HD
- Nucleasi a dita di zinco, un modo possibile per correggere le mutazioni del DNA
- Neuroni di cellule staminali: creare le giuste connessioni
Fonti e Riferimenti
Per maggiori informazioni sulla nostra politica di divulgazione, consulta le nostre FAQ…


